
News information
分类:行业资讯 发布时间:2023-05-25 访问量:856
5月17日,国家药监局发布最新药品批准证明文件。
其中,齐鲁制药的奥拉帕利片获批上市,为国内首仿。
奥拉帕利(olaparib)是一款口服多腺苷二磷酸核糖聚合酶(PARP)抑制剂。通过抑制PARP,减少甚至阻止携带有受损BRCA基因的癌细胞进行DNA修复,达到杀死癌细胞死亡的目的。而卵巢癌患者大约60%存在DNA同源重组缺陷,其中20%属于BRCA1/2突变。PARP抑制剂的出现,对部分肿瘤的药物治疗方案带来了革命性的变化,尤其适用于卵巢癌,使复发性卵巢癌的药物治疗迈入了精准治疗时代,被誉为“里程碑式的靶向药”。
奥拉帕利(olaparib)原研企业是阿斯利康。奥拉帕利片最早于2014年先后在欧盟和美国获批上市,商品名为Lynparza。截至目前,奥拉帕利已在各地区相继获批卵巢癌、乳腺癌、去势抵抗性前列腺癌、胰腺癌、输卵管癌、腹膜癌等多项适应症。
2017年7月,默沙东与阿斯利康达成战略合作,共同开发和推广Lynparza,平分销售额,涉及交易金额达85亿美元。
阿斯利康的奥拉帕利近年来销售额稳定增长,2019年全球销售额为11.98亿美元,2020年为17.76亿美元;2021年为23.48亿美元,2022年最新销售额达26.38亿美元,同比增长12.4%,位列全球药物销售榜单54位。
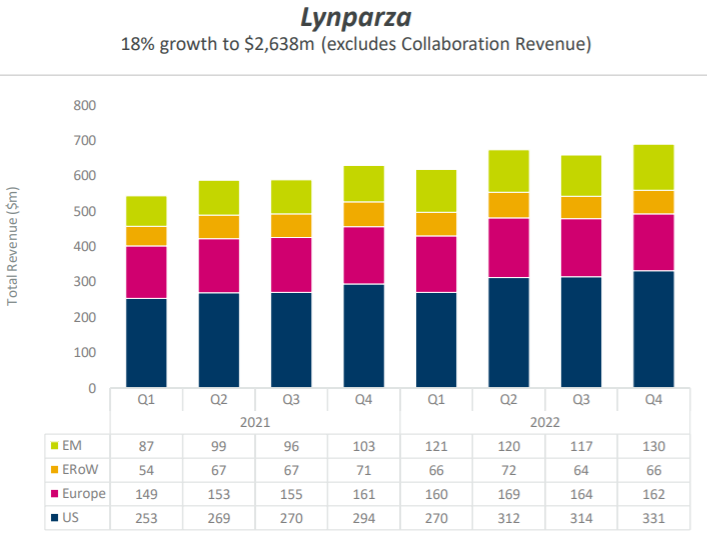
(来源:阿斯利康财报)
在国内,奥拉帕利于2018年8月首次获NMPA批准上市,商品名为利普卓,是国内首个上市的PARP抑制剂,同时填补了国内卵巢癌靶向新药治疗领域近30年的空白。在国内获批的适应症有:
1.铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗;
2.携带胚系或体细胞BRCA突变(gBRCAm或sBRCAm)晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌初治成人患者在一线含铂化疗达到完全缓解或部分缓解后的维持治疗;
3.单药用于治疗携带胚系或体细胞BRCA突变(gBRCAm或sBRCAm)且既往治疗(包括一种新型内分泌药物)失败的转移性去势抵抗性前列腺癌成人患者;
4.奥拉帕利联合贝伐珠单抗用于同源重组修复缺陷(HRD)阳性的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在一线含铂化疗联合贝伐珠单抗治疗达到完全缓解或部分缓解后的维持治疗,该适应症于2022年9月获批。
奥拉帕利于2019年通过谈判纳入全国医保乙类目录,从24790元/盒降到9464元/盒。根据最新的2022年医保目录,奥拉帕利通过医保谈判新增加了前列腺癌适应症,目前国内获批的前3个适应症均成功纳入国家医保目录。而且值得一提的是,最新医保价格已经降到5026元/盒。
根据米内网数据,奥拉帕利进入医保后销售规模节节高升,2021年中国三大终端六大市场销售额突破10亿元,2022年已上涨至超13亿元,医保扩大适应症后有望进一步上涨。
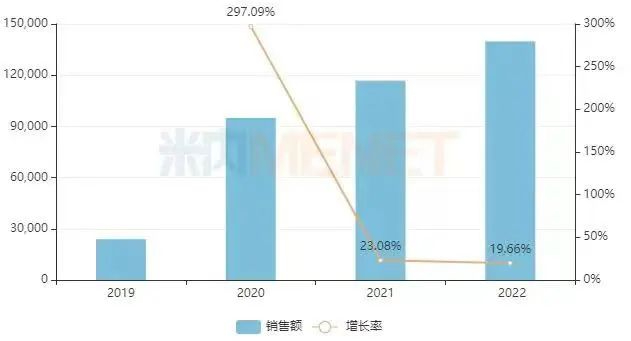
(来源:米内网)
自2014年首款PARP抑制剂上市至今,全球范围已有6款PARP抑制剂相继上市。目前国内已有4款PARP抑制剂获批,除了奥拉帕利,还有尼拉帕利(再鼎药业)、氟唑帕利(恒瑞医药)和帕米帕利(百济神州),2022年国内销售规模合计超过25亿元,其中奥拉帕利的销售额最高,占比达54%。
最早在国内布局奥拉帕利的仿制厂商为齐鲁制药,于2021年10月提交上市申请并获受理,历时约一年半获批上市,拿下首仿。
从2022年到现在,又有7家企业相继提交了上市申请,分别为上海宣泰医药科技、湖南科伦制药、石药集团欧意药业、杭州中美华东制药、南京方生和医药科技、江西山香药业和Natco Pharma(进口5.2类)。另外还有一些药企正在开展奥拉帕利的BE试验。相关仿制药上市后将惠及更多患者,提供更多治疗选择。
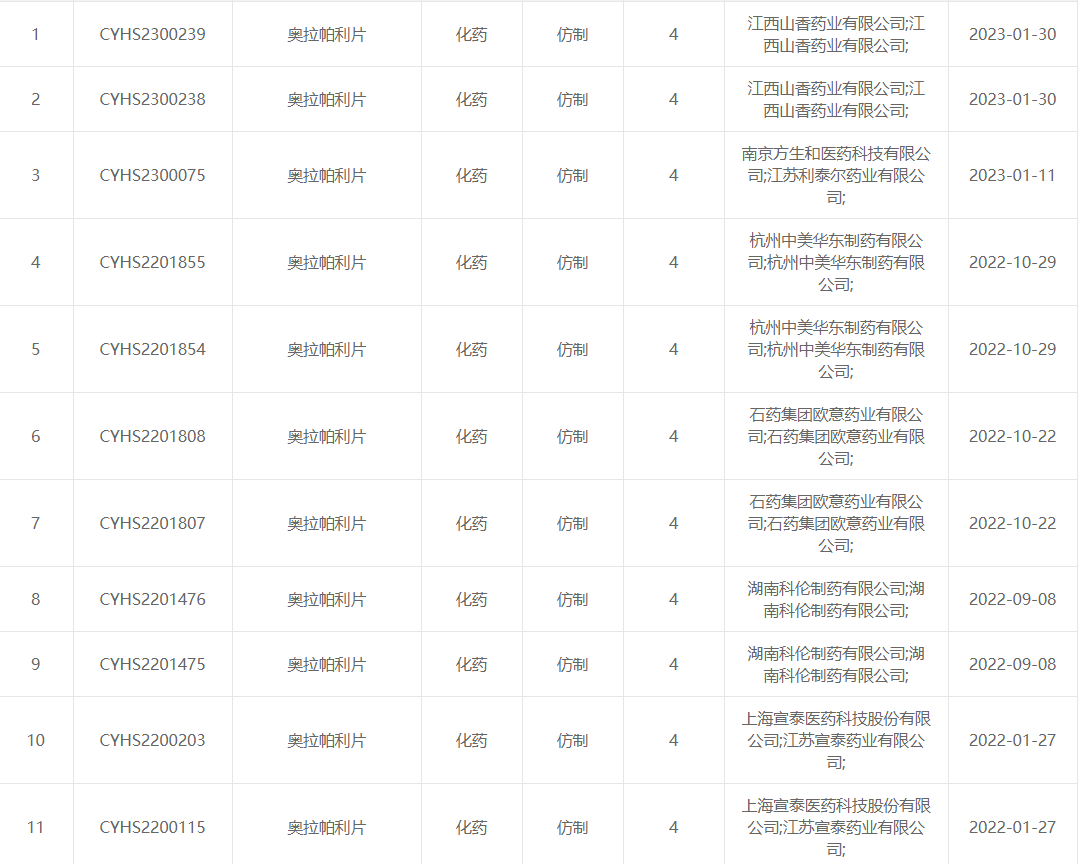
(来源:CDE官网)
另外,根据CDE专利登记平台,奥拉帕利化合物专利将于2024年3月到期,齐鲁制药已在CDE专利登记平台发表声明,承诺在相应专利权有效期届满之前所申请的仿制药暂不上市销售。
来源于网站,如有侵权请联系删除。

国家医保部门从多个方面考虑到参保人员的利益,进而对相关政策进行调整和完善,提升居民的生活幸福感。

2020年-2025年,因新品上市以及患癌人数不断增加,因此从市场规模也随之上升。根据头豹研究院整理,ADC药物的市场规模预计在2024年有望达到74 亿元,2030年预计市场规模达到292亿元人民币,2024-2030年复合增长率为25.71%。

国家卫生健康委发布最新公告显示,2020年各类传播途径的甲乙类传染病发病率均呈现明显下降,其中肠道传染病发病率较2019年下降29.4%、呼吸道传染病发病率较2019年下降12.9%。因此,全球,包括中国在内的抗菌药物的使用额呈下降趋势。
随着新药的不断研发和政策的完善,渐冻症治疗市场有望迎来更加广阔的发展前景。