
News information
分类:行业资讯 发布时间:2023-08-02 访问量:1095
背 景
针对突变基因使用靶向药物,相比于过去使用的化疗药物生存期得到明显改善。靶向药物治疗基因突变的非小细胞肺癌,有效率在70%以上,控制肿瘤的时间是化疗的两倍,并且副作用小,生活质量高。
肺癌EGFR突变在一定程度上,保证在毒副作用小的前提下,有效延缓患者生存情况,并且,由于靶向TKI药物的特性,可以保证让人们不接受费时、费力的化疗,这大大提升了患者的生活质量和水平。
EGFR是什么?
EGFR基因称为表皮生长因子受体,就是表皮细胞表面的受体,接收生长因子的信号,向细胞内传递,通过一系列信号传递过程,促进细胞的生长。它对于细胞的生长与凋亡有重要作用,在各个部位的表皮需要细胞分裂补充的时候,EGFR基因就会活跃起来,开始运转,表达出EGFR,放在细胞表面接收生长信号,使用完后就会关闭生产线。
表皮生长因子受体(EGFR)是能与受体酪氨酸激酶(RTK)结合的细胞生长因子包括:EGFR(ErbB-1)、2型人表皮生长因子受体HER2(ErbB-2)、3型人表皮生长因子受体HER3(ErbB-3)及4型人表皮生长因子受体HER4(ErbB-4)。其中,EGFR和HER2是EGFR家族成员中与肿瘤关系最为密切的靶点。
研究表明,肿瘤细胞的生长、增殖、分化及凋亡与EGFR基因的异常表达有关,EGFR信号通路对细胞的生长、增殖和分化等生理过程发挥重要的作用,可以达到抗肿瘤的目的。
EGFR 突变与癌症的关联
研究表明在许多实体肿瘤中存在EGFR的高表达或异常表达。EGFR与肿瘤细胞的增殖、血管生成、肿瘤侵袭、转移及细胞凋亡的抑制有关。
EGFR的过表达在恶性肿瘤的演进中起重要作用,胶质细胞、肾癌、肺癌、前列腺癌、胰腺癌、乳腺癌等组织中都有EGFR的过表达。对胶质细胞瘤的研究发现EGFR的高表达主要与其基因扩增有关。
突变型EGFR的作用可能包括:具有配体非依赖型受体的细胞持续活化;由于EGFR的某些结构域缺失而导致受体下调机制的破坏、异常信号传导通路的激活、细胞凋亡的抑制等。突变体的产生是由于EGFR基因的缺失、突变和重排。
EGFR的配体对细胞内信号传导有很大影响。EGFR的配体通过自分泌形式激活EGFR促进细胞增殖,他们的共表达往往预示肿瘤预后不良。
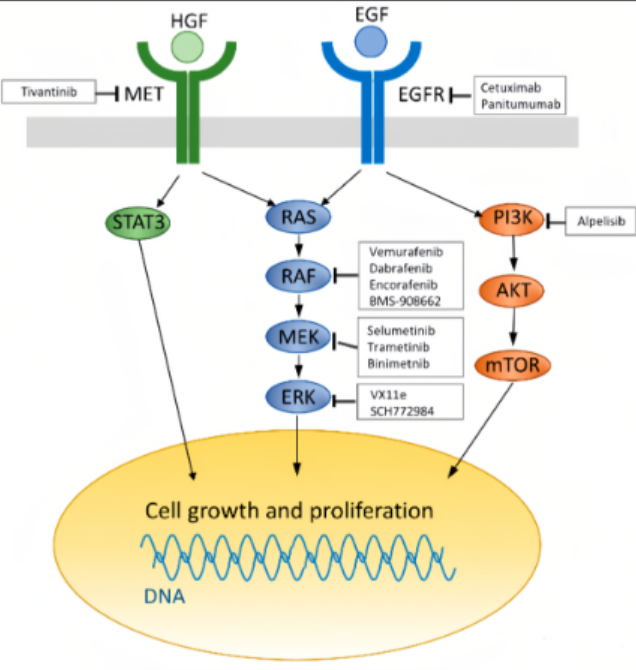
EGFR信号过表达导致肿瘤发生
上世纪八十年代以来,发现多种上皮来源的实体肿瘤组织如非小细胞肺癌、结直肠癌、胰腺癌、肾癌、膀胱癌,存在EGFR高表达的现象,并且此部分患者预后不佳,提示EGFR过度传递生长信号可能是肿瘤发生发展的原因之一。
经过多年的研究,发现EGFR以下几种形式导致生长信号过度表达,并对机体分泌的抗生长信号不敏感。
①信号源过表达,如EGF,HGF等生长因子高表达。
②EGFR自身过表达,如拷贝数增多。
③EGFR突变导致生长信号活化。
④下游信号通路活化突变,如KRAS,BRAF突变等。
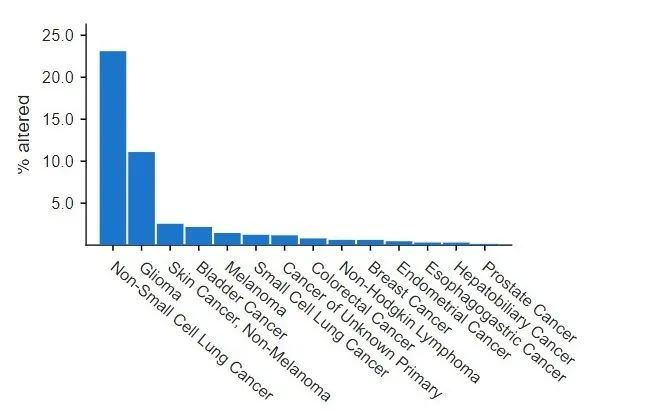
EGFR在不同癌种的突变率
EGFR靶向药物的治疗机理
治疗机理是阻断EGFR的效用,从而抑制信号转导。目前有两类药物:
EGFR-TKI药物
TKI是酪氨酸激酶抑制剂,为一类能抑制酪氨酸激酶活性的化合物。酪氨酸激酶抑制剂主要通过抑制细胞信号转导而抑制肿瘤细胞的生长和增殖,促进细胞凋亡。
目前EGFR酪氨酸激酶抑制剂(EGFR-TKI)已经发展到了三代,第四代EGFR-TKI如BLU-945等已进入临床研究。
EGFR单抗
西妥昔单抗、帕尼单抗、耐昔妥珠单抗和尼妥珠单抗等药物。
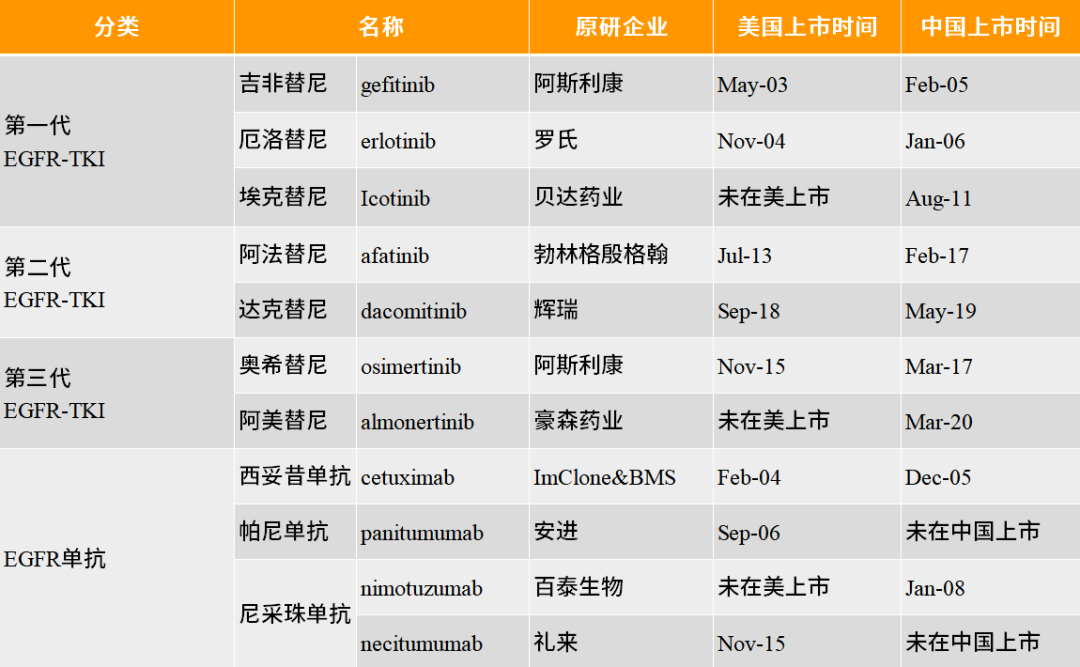
总结

国家医保部门从多个方面考虑到参保人员的利益,进而对相关政策进行调整和完善,提升居民的生活幸福感。

2020年-2025年,因新品上市以及患癌人数不断增加,因此从市场规模也随之上升。根据头豹研究院整理,ADC药物的市场规模预计在2024年有望达到74 亿元,2030年预计市场规模达到292亿元人民币,2024-2030年复合增长率为25.71%。

国家卫生健康委发布最新公告显示,2020年各类传播途径的甲乙类传染病发病率均呈现明显下降,其中肠道传染病发病率较2019年下降29.4%、呼吸道传染病发病率较2019年下降12.9%。因此,全球,包括中国在内的抗菌药物的使用额呈下降趋势。
随着新药的不断研发和政策的完善,渐冻症治疗市场有望迎来更加广阔的发展前景。