
News information
分类:行业资讯 发布时间:2023-05-25 访问量:751
据报道,10%至20%的非小细胞肺癌NSCLC患者在首次诊断时合并脑转移(BM),而25%至50%的NSCLC患者最终会在病程中发展为BM,值得注意的是,每3名EGFR+ NSCLC患者中就有1名在其临床过程中发生脑转移 。虽然EGFR-TKI的全身治疗被推荐作为EGFR突变的晚期NSCLC患者的一线治疗,但不同药物的颅内活性不同。因此,在选择治疗方案时应考虑脑转移 (BM)。近日,《中国医学杂志》发表一项网络荟萃分析,旨在探索具有不同BM状态的晚期EGFR突变NSCLC患者的最佳一线治疗方案。
研究人员系统地检索了截至2021年12月针对未接受系统治疗的晚期、EGFR突变NSCLC患者使用EGFR-TKI(单独或联合)的随机对照试验。提取并分析了PFS和OS。该分析包括17项随机对照试验,涉及5077名患者和12种疗法,包括奥希替尼+贝伐珠单抗、阿美替尼、奥希替尼、阿法替尼、达克替尼、护理标准(SoC,包括吉非替尼、厄洛替尼或埃克替尼)、SoC + 阿帕替尼、SoC + 贝伐珠单抗、SoC + ramucirumab、SoC + 基于培美曲塞的化疗 (PbCT)、PbCT 和无培美曲塞化疗 (PfCT)。
结果显示:奥希替尼+贝伐珠单抗最有可能在伴或不伴BM的晚期EGFR突变NSCLC患者的PFS中排名第一,而SoC+PbCT最有可能在OS中排名第一。
针对肺癌脑转,靶向TKI精准拿捏
1、EGFR突变伴脑转移,怎么办?
优选三代EGFR-TKI药物,其次是一代EGFR-TKI,最后是二代EGFR-TKI。
奥希替尼
在第一代EGFR-TKI中,与吉非替尼相比,厄洛替尼具有相对更好的穿越血脑屏障的能力。在吉非替尼治疗后出现脑转移/软脑膜疾病的一些患者中,改用厄洛替尼可导致颅内肿瘤缩小或症状缓解。但是,效果通常是短暂的。厄洛替尼的脉冲高剂量和剂量递增也被证明可以更有效地控制脑转移,但疗效有限。
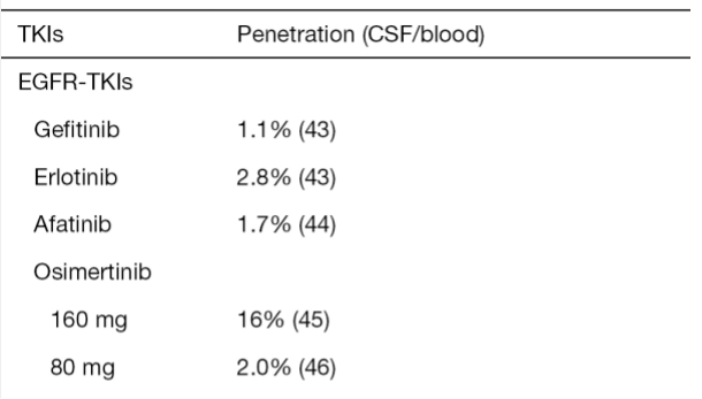
相比之下,第三代EGFR-TKI,奥希替尼更有效地穿透BBB。FLAURA试验结果的子集分析将奥希替尼与吉非替尼或厄洛替尼作为EGFR+患者的一线治疗进行了比较,结果表明奥希替尼的CNS无进展生存期明显更好 [风险比 (HR) 0.48;95% CI:0.26–0.86],具有可控的不良反应。
阿美替尼
2023年ELCC上,研究人员分享了一项前瞻性II期研究(NCT04519983)的最新结果。在颅内寡转移性EGFR突变的非小细胞肺癌(NSCLC)患者中,给予阿美替尼联合立体定向放射治疗(SRT),产生较好的中枢神经系统(CNS)反应。可评估疗效的患者(n= 32)颅内客观缓解率(iORR)为100%,其中3例完全缓解(CR)和29例部分缓解(PR)。颅内疾病控制率(iDCR)也为100%。
伏美替尼
治疗EGFR T790M突变阳性伴脑转移NSCLC患者的颅内ORR为65.2%,颅内DCR为91.3%,颅内中位PFS未达到;其中160 mg剂量组的颅内ORR为84.6%,颅内中位PFS为19.3个月。
2、ALK融合阳性的患者,怎么办?
众所周知, ALK基因重排的患者脑转移风险更高,初始评估时为 23.8%。诊断后脑转移的累积发生率在3年后总和为 58.4%。
目前,有五种ALK-TKI被FDA批准用于ALK阳性NSCLC,即克唑替尼(第一代)、阿来替尼、塞瑞替尼、布加替尼(第二代)和劳拉替尼(第三代)。值得注意的是,高达74%接受克唑替尼治疗的患者发生了脑转移。与克唑替尼相比,第二代TKI 具有更好的穿透 BBB 和控制脑转移的能力。

ALEX试验显示阿来替尼对先前未治疗的脑转移有81%的颅内反应,而克唑替尼的反应率为50%。经克唑替尼一线治疗后复发的患者,使用塞瑞替尼(45%)和布加替尼(42–67%)也获得了高颅内反应。在TKI中,与克唑替尼相比,第二代ALK-TKI 在前线显示出更好的存活率 。据报道,第二代ALK-TKI的颅内ORR几乎比第一代TKI克唑替尼高2到3倍,现在被定位为脑转移NSCLC的一线药物。与厄洛替尼相似,阿来替尼剂量递增疗法实现了ALK抑制,正在等待临床批准。第三代ALK-TKI劳拉替尼在一线克唑替尼后复发的患者中也表现出42-48%的颅内反应。ALK-TKI用于有效疾病控制的顺序需要进一步评估。
3、ROS1突变融合阳性,怎么办?
克唑替尼
克唑替尼为目前中国唯一批准的ROS1-TKI,可以作为NSCLC脑转移患者的治疗选择。
恩曲替尼
ALKA-372-001、STARTRK-1和STARTRK-2临床研究的汇总结果显示,恩曲替尼用于ROS1融合基因阳性NSCLC脑转移患者的颅内ORR为55.0%。
除靶向TKI“条条大道通罗马”
1、抗血管生成药物
一项贝伐珠单抗治疗NSCLC脑转移患者的荟萃分析结果显示,与对照组相比,贝伐珠单抗治疗组的疗效更好,经贝伐珠单抗治疗的患者颅内病灶的ORR和DCR均优于颅外病灶,且不增加脑转移患者的出血风险。除此之外,贝伐珠单抗对于放射治疗导致的脑坏死和脑水肿也有一定效果,多项研究表明,贝伐珠单抗可以在一定程度上减轻脑水肿。
2、化疗
以铂类药物为基础,联合培美曲塞、长春瑞滨 等药物可给NSCLC脑转移患者带来生存获益。GFPC07-01研究纳入初治NSCLC脑转移患者,顺铂联合培美曲塞治疗脑转移病灶的ORR为41.9%,颅外病灶的ORR为34.9%,中位OS为7.4个月。替莫唑胺是一种新型咪唑四嗪类烷化剂,能透过血脑屏障,对于控制NSCLC脑转移有较好的疗效。但由于样本量较少,尚需大规模的Ⅲ期临床研究进一步证实。
3、免疫治疗
K药:治疗PD-L1阳性脑转移患者,颅内ORR达29.7%!
2020年4月3日,在《柳叶刀》发表了PD1单抗K药治疗有脑转移的NSCLC(非小细胞肺癌)患者的II期前瞻性研究结果,这也是首个免疫治疗脑转移的针对性研究。该研究共纳入42例患者:队列1为PDL1阳性患者,有37例;队列2为PDL1表达未知的经治患者,有5例。8例患者(20%)伴有敏感基因突变如EGFR、ALK或HER2突变。64%患者既往接受过系统性治疗。50%患者未针对颅内病灶进行过治疗(如放疗)。
中位随访时间为8.3个月,结果显示,队列1中11例PD-L1阳性患者发生反应,颅内ORR(客观缓解率)为29.7%,其中4例达到颅内完全缓解(CR),7例部分缓解(PR),4例达到颅内疾病稳定(SD)。
在队列1的37例患者中,总体(颅内和颅外都缓解)ORR为18.9%,颅外ORR为29.7%,颅外中位DOR为6.9个月。有6例患者出现颅内及颅外不一致的反应,只有颅内或颅外缓解的患者各3例。所有反应不一致的患者都存活了6个月以上,2例(2/3)颅内进展,但颅外缓解的患者存活了2年以上。
中位PFS为1.9个月,颅内PFS为2.3个月,33%患者的颅内无进展时间超过1年。中位OS(总生存期)为9.9个月,估计1年总生存率 40%,2年生存率为34%。对于脑转移NSCLC患者,既往的数据显示2年生存率只有14.3%,而K药治疗的2年生存率明显提高到34%,这样的结果非常令人鼓舞!说明K药治疗脑转具备一定的潜力。
O药:治疗脑转,疗效也不降档
这项研究发布在Lung Cancer杂志,分析了在意大利用PD1单抗O药(纳武利尤单抗)后线治疗NSCLC脑转移患者的真实世界疗效。该试验共纳入了1588例NSCLC患者,共409例患者在基线就有脑转移,占了超过四分之一(26%)。这409例患者中,有29%用过激素治疗,18%用激素同步放疗,59%做过脑部放疗。值得注意的是,这些患者都是在多次治疗失败后用O药,其中既往接受过治疗线数≥3次的患者就占了46%。
结果显示,脑转移患者的ORR为17%,DCR为39%,其中有4例出现完全缓解(CR)。脑转移患者的疗效与总体人群的疗效非常接近(总人群ORR为18%,DCR为44%)。
脑转患者的中位PFS为3个月,与总人群相同。脑转患者的中位OS及1年OS率为8.6个月和20%,而总人群的中位OS为11.3个月、1年OS率为43%。有脑转患者的生存期相对短一些,但是后线OS还能达到8.6个月已经算是不错了。
T药:OAK研究显示有延长生存时间的趋势
OAK研究纳入了经治晚期NSCLC患者,接受PDL1单抗T药(阿替利珠单抗)或多西他赛治疗。两组约有14%的患者在入组时判断为无症状脑转。在脑转患者中,两组分别有90.2%(阿替利珠单抗)及82.3%(多西他赛)的患者接受过脑部放疗。
结果显示,有脑转史的患者,T药组的中位OS优于化疗组,为16m vs 11.9m,但无统计学差异(P=0.16);无脑转史的患者中T药组的中位OS明显优于化疗组(13.2m vs 9.3m,P=0.0007)。
另外,有脑转史的患者中,T药组的患者出现新发脑转移灶中位时间比化疗组更长,为未达到vs 9.5个月。无脑转史患者中,两组出现新发脑转移灶中位时间都未达到。
I药:PACIFIC研究将脑转移发生率降低一倍!
PACIFIC试验是一个随机、双盲、多中心的III期试验,患者在同步放化疗后序贯Durvalumab(I药,英飞凡)或安慰剂。I药除了在ORR、PFS及OS都优于安慰剂外,有新数据显示,两组出现新病灶的发生率为I药 22.5% vs安慰剂33.8%。重点是对于严重影响预后的脑转移发生率,I药组比安慰剂低(6.3% vs 11. 8%),I药明显降低了高风险转移灶的发生。
除了上述的药物治疗,手术切除、全脑放疗(WBRT)、立体定向放疗(SRT)对于脑转移病灶同样重要,联合系统药物治疗可以更好的改善患者症状和生活质量,最大程度地延长患者的生存时间。
来源于网站,如有侵权请联系删除。

国家医保部门从多个方面考虑到参保人员的利益,进而对相关政策进行调整和完善,提升居民的生活幸福感。

2020年-2025年,因新品上市以及患癌人数不断增加,因此从市场规模也随之上升。根据头豹研究院整理,ADC药物的市场规模预计在2024年有望达到74 亿元,2030年预计市场规模达到292亿元人民币,2024-2030年复合增长率为25.71%。

国家卫生健康委发布最新公告显示,2020年各类传播途径的甲乙类传染病发病率均呈现明显下降,其中肠道传染病发病率较2019年下降29.4%、呼吸道传染病发病率较2019年下降12.9%。因此,全球,包括中国在内的抗菌药物的使用额呈下降趋势。
随着新药的不断研发和政策的完善,渐冻症治疗市场有望迎来更加广阔的发展前景。