
News information
分类:行业资讯 发布时间:2023-07-06 访问量:1144
2023年上半年已结束。据不完全统计,截至6月30日,今年有将近50款新药首次获得中国国家药监局(NMPA)批准上市,其中大约76%为小分子化药,此外还有多款生物药。
从治疗领域来看,这些新药仍以抗肿瘤产品居多,其次是罕见病和抗感染领域治疗产品。值得一提的是,有将近37%的新药是得益于优先审评、附条件批准等政策,加速来到了患者身边。
与此同时,2023上半年还有30多款新药在中国迎来了新适应症,包括多款JAK抑制剂和抗PD-1单抗。此外,还有多款生物类似药也在中国获批。
本文中,就让我们来一起看看今年上半年在中国获批的新药都有哪些?它们都惠及了哪些患者?
40多款新药首次获批
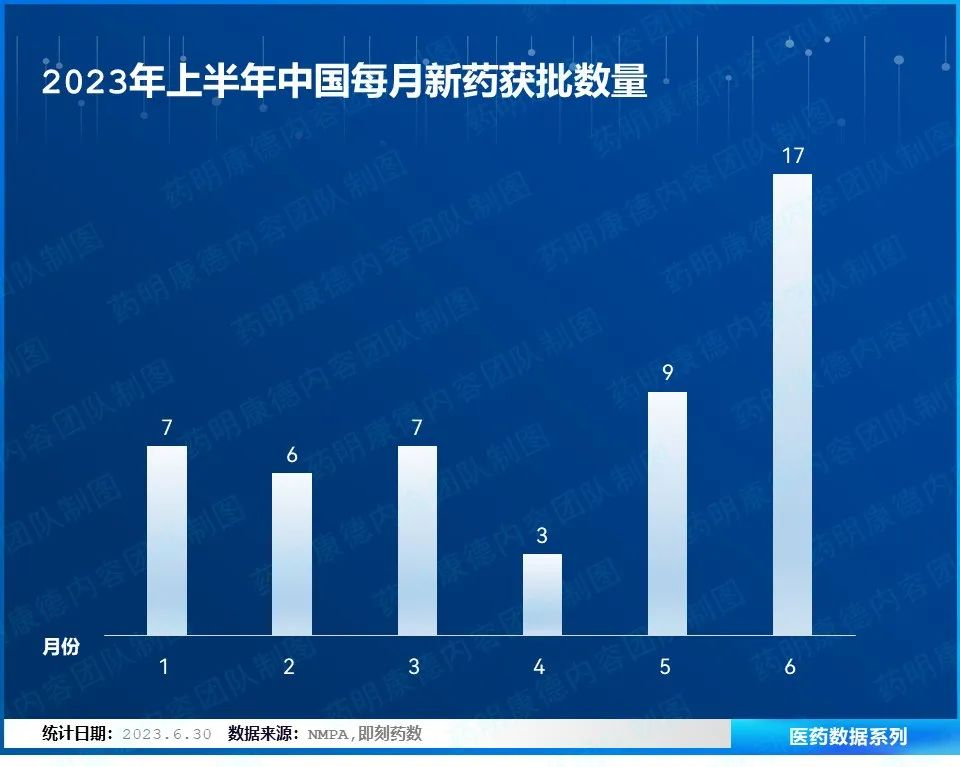
根据NMPA官网批件信息,上半年共有近50款新药在中国首次获批,其中6月份获批新药数量最多,达到17款。
从药物获批类型来看,小分子新药占比约76%,包括针对CDK4/6、MET、BTK、MEK、PI3K、DPP-4、ALK等靶点的创新抑制剂等。
此外,还有12款生物药在中国获批,包括CAR-T产品、ADC、GLP-1RA复方制剂、长效粒细胞集落刺激因子(G-CSF)、单克隆抗体等等。

梳理这些获批新药,我们发现多款产品创下了“首个”获批的记录,为患者带来了全新的治疗选择。例如:
武田(Takeda)琥珀酸莫博赛替尼胶囊
全球首个获批治疗EGFR 20号外显子插入突变患者的口服靶向药物,本次在中国获批治疗EGFR 20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC);
罗氏(Roche)注射用维泊妥珠单抗
全球首个获批的靶向CD79b的ADC,本次在中国获批治疗治疗弥漫性大B细胞淋巴瘤(DLBCL)成人患者;
驯鹿生物与信达生物联合开发的伊基奥仑赛注射液
中国首款获批的BCMA靶向CAR-T产品,本次获批治疗复发或难治性多发性骨髓瘤(MM)成人患者;
阿斯利康(AstraZeneca)和默沙东(MSD)共同开发的MEK抑制剂司美替尼
中国首个获批的I型神经纤维瘤病(NF1)治疗药物;
北海康成引进的IBAT抑制剂迈芮倍口服液
中国首个获批治疗阿拉杰里综合征(ALGS)患者胆汁淤积性瘙痒的药物
从治疗领域来看,上半年获批的新药仍以抗肿瘤产品居多,而从癌症细分适应症来看,获批最多的是肺癌药物,同时在罕见病领域和抗感染领域也有许多新药获批。
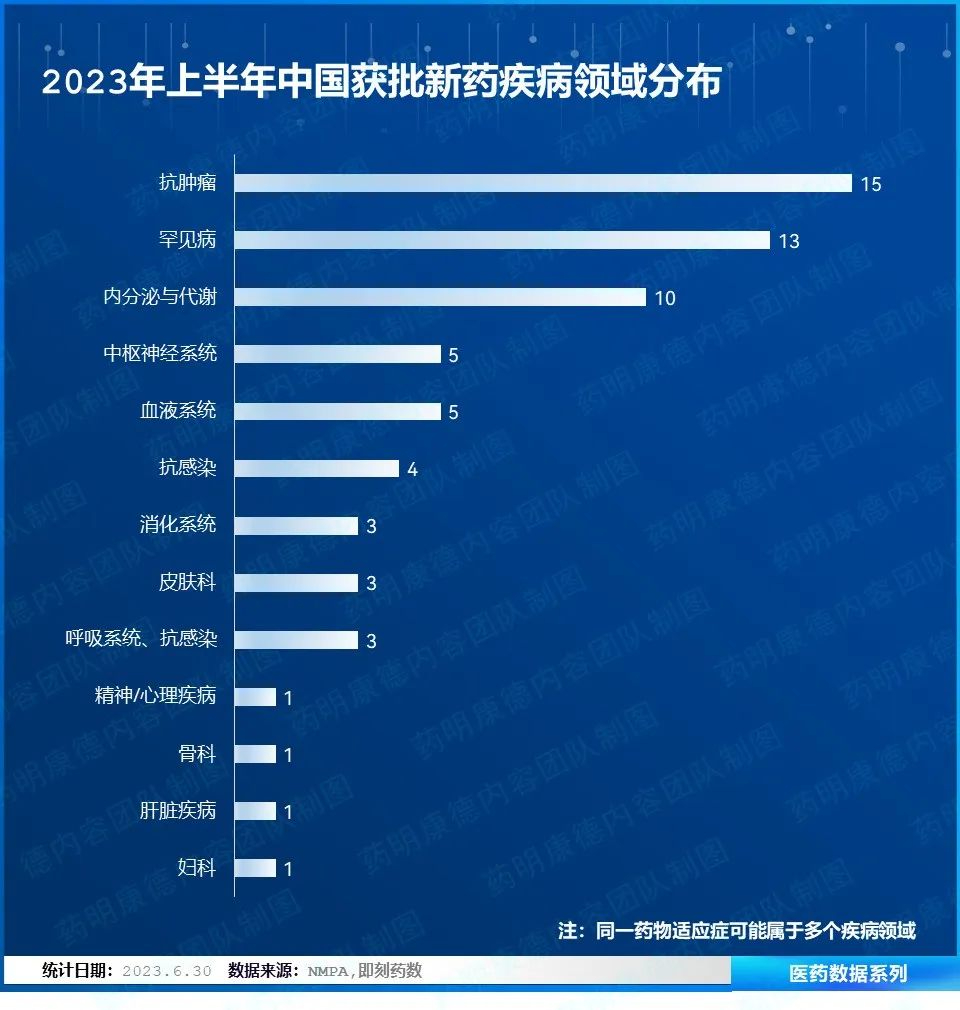
肿瘤/癌症领域
在肺癌治疗领域,齐鲁制药ALK/ROS1抑制剂伊鲁阿克、海和药物MET抑制剂谷美替尼贝达药业第三代EGFR-TKI贝福替尼等,均获批治疗非小细胞肺癌;恒瑞医药抗PD-L1单抗阿得贝利单抗则获批治疗广泛期小细胞肺癌。
在淋巴瘤治疗领域,上半年也迎来了4款新药,分别是阿斯利康新一代BTK抑制剂阿可替尼、拜耳(Bayer)PI3K抑制剂可泮利塞、罗氏ADC疗法维泊妥珠单抗和博锐生物抗CD20单抗泽贝妥单抗。
在乳腺癌领域,诺华(Novartis)CDK4/6抑制剂琥珀酸瑞波西利片和阿斯利康和第一三共(Daiichi Sankyo)联合开发的HER2靶向ADC注射用德曲妥珠单抗的获批也为患者带来了新选择。
此外,肾细胞癌领域也迎来了贝达药业的多靶点激酶抑制剂伏罗尼布。
抗感染治疗领域
抗感染是另一获批新药较多的治疗领域
其中包括:恒瑞医药引进的抗真菌新药奥特康唑胶囊、吉利德科学(Gilead Sciences)侵袭性真菌病一线治疗产品注射用两性霉素B脂质体、云顶新耀治疗成人复杂性腹腔内感染的注射用盐酸依拉环素、圣和药业治疗慢性丙型肝炎病毒感染的奥磷布韦等。
同时,还有3款新药获批用于治疗治疗新型冠状病毒感染(COVID-19),分别来自先声药业、旺实生物和众生药业。
罕见病领域
在罕见病领域,上半年也迎来多款新药,为不同类型的罕见病患者带来治疗希望。
除了上文提及的司美替尼和氯马昔巴特口服溶液,另外还有:百时美施贵宝公司的奥扎莫德和梯瓦(Teva)公司的醋酸格拉替雷均获批治疗多发性硬化、苏庇医药尼替西农获批治疗1型遗传性酪氨酸血症、维健医药引进的苯丁酸甘油酯获批用于尿素循环障碍患者的长期治疗、Recordati子公司锐康迪卡谷氨酸分散片获批治疗多种罕见高氨血症、希而欧生物西罗莫司凝胶获批用于治疗结节性硬化症皮肤损害等。
30多款新药收获新适应症
除了首次获批的新药,2023上半年还有30多款新药在中国获批新适应症。
其中,小分子占比约61%,包括针对BTK、JAK、SGLT2、CDK4/6、TKs、RET等靶点的抑制剂;生物药占比约39%,主要是针对PD-1、RANKL、VEGF、CD38、TNF-α、EGFR、IL-12/IL-23、IL-4/IL-13、IgE等靶点的单抗类产品,以及靶向CD19的CAR-T产品、GnRH类似物等。
从药品作用机制来看,抗PD-1单抗斩获新适应症最多。
来自百时美施贵宝、康方生物/正大天晴、复宏汉霖、百济神州、信达生物和恒瑞医药等公司的6款抗PD-1单抗共计斩获8项新适应症,涵盖小细胞肺癌、非小细胞肺癌、尿路上皮癌、胃或胃食管结合部腺癌、食管鳞状细胞癌、肝细胞癌等不同瘤种。
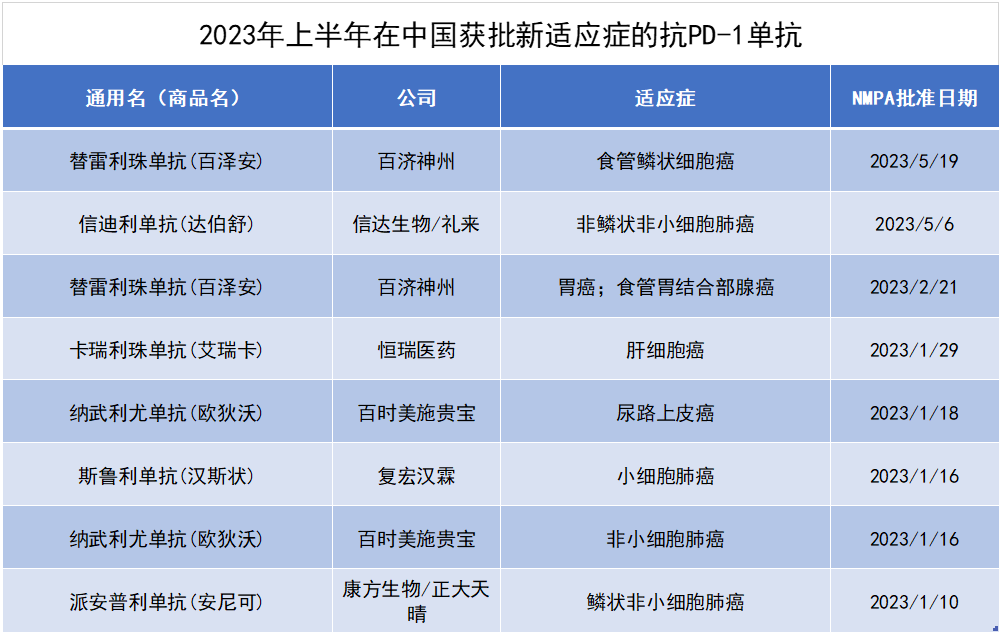
其次是小分子JAK抑制剂,来自辉瑞(Pfizer)枸橼酸托法替布缓释片、艾伯维(AbbVie)乌帕替尼缓释片、礼来(Eli Lilly and Company)巴瑞替尼片、诺华磷酸芦可替尼片等4款JAK抑制剂的新适应症上市申请先后在中国获批,治疗溃疡性结肠炎、急性移植物抗宿主病、斑秃等疾病。
值得一提的是,巴瑞替尼片斑秃适应症的获批,使其成为中国首款用于系统性治疗重度斑秃的创新靶向药物,为中国重度斑秃患者带来获得显著毛发再生的治疗新选择。
此外,还有多种靶向疗法获批新适应症,根据不同疾病领域划分有:
肿瘤领域
肿瘤领域有恒瑞医药TKI新药吡咯替尼和阿帕替尼及CDK4/6抑制剂羟乙磺酸达尔西利片、基石药业RET抑制剂普拉替尼、复星凯特CD19靶向CAR-T产品阿基仑赛注射液、百济神州BTK抑制剂泽布替尼、诺诚健华BTK抑制剂奥布替尼、诺华CDK4/6抑制剂瑞波西利、拜耳雄激素受体抑制剂(ARi)达罗他胺、百泰生物抗EGFR单抗尼妥珠单抗等获批不同肿瘤适应症,涵盖肺癌、乳腺癌、淋巴瘤、胃癌、肝癌、胰腺癌、前列腺癌等;
皮肤科领域
皮肤科领域有杨森IL-12/IL-23抑制剂乌司奴单抗获批治疗儿童银屑病,赛诺菲/再生元(Regeneron)IL-4/IL-13抑制剂度普利尤单抗获批治疗婴幼儿特应性皮炎,诺华奥马珠单抗预充式注射液获批治疗慢性自发性荨麻疹等;
内分泌和代谢领域
内分泌和代谢领域,有益普生(IPSEN)GnRH类似物注射用双羟萘酸曲普瑞林获批治疗性早熟等群体;勃林格殷格翰(Boehringer Ingelheim)/礼来SGLT2抑制剂恩格列净获批糖尿病新适应症;拜耳非甾体选择性盐皮质激素受体拮抗剂非奈获批拓展适应症至慢性肾脏病早期阶段;
罕见病领域
在罕见病领域,有罗氏SMN2基因mRNA剪接修饰剂利司扑兰口服溶液用散获批治疗脊髓性肌萎缩症(SMA),阿斯利康C5补体抑制剂依库珠单抗注射液获批全身型重症肌无力等;
抗感染领域
在抗感染领域,有葛兰素史克(GSK)HIV新药多替拉韦钠分散片获批治疗儿童患者;
骨科领域
在骨科领域,有安进抗RANKL单抗地舒单抗获批治疗男性骨质疏松症;
神经或精神领域
在神经或精神领域,有大冢制药(Otsuka Pharmaceutical)非典型抗精神病药物注射用阿立哌唑等;
此外,还有益普生注射用双羟萘酸曲普瑞林六月超长效剂型、卫材(Eisai)抗癫痫药吡仑帕奈口服混悬液等新剂型获批等。
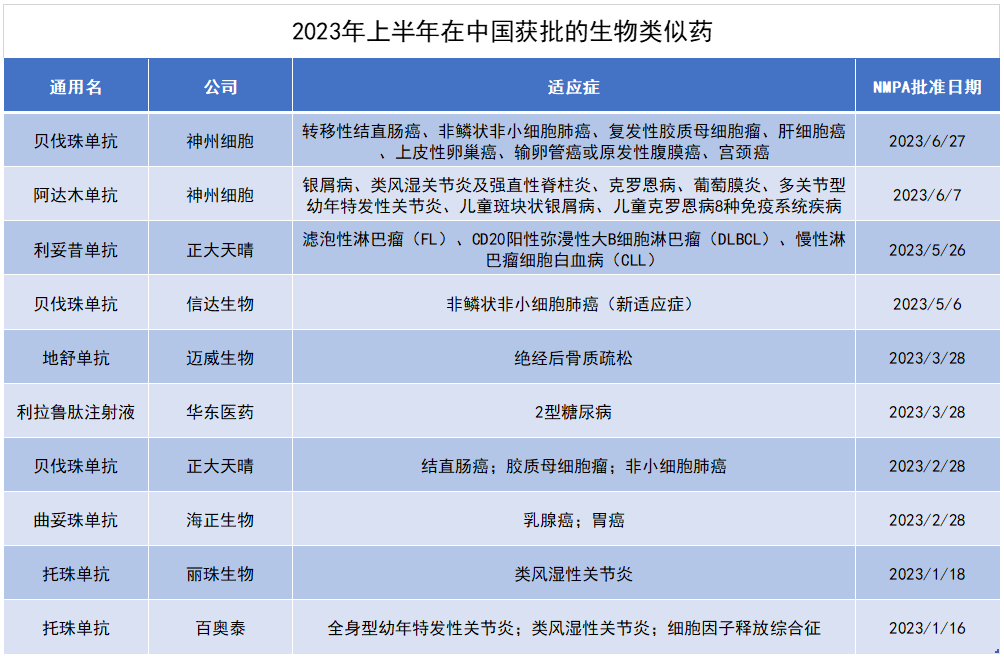
40多款新药多款生物类似药陆续获批首次获批
近年来,由中国公司开发的生物类似药陆续获批上市,一些产品还实现了海外授权。
在今年上半年NMPA批准的产品中,9款生物类似药首次获批,1款生物类似药获批新适应症。
这些产品有阿达木单抗、贝伐珠单抗、地舒单抗、利拉鲁肽注射液、利妥昔单抗、曲妥珠单抗、托珠单抗等,获批适应症包括癌症、自身免疫性疾病等(详见下表)。
总结
2023年上半年,我国新获批药物越来越多新药在中国获批,覆盖肿瘤、抗感染、罕见病等多个领域,其中肿瘤类药物最多,其次为罕见病药物。新药获批再创新高,加上优先审评、附条件批准等政策,让更多创新药加速来到患者身边,造福更多的患者。
来源于网站,如有侵权请联系删除。

国家医保部门从多个方面考虑到参保人员的利益,进而对相关政策进行调整和完善,提升居民的生活幸福感。

2020年-2025年,因新品上市以及患癌人数不断增加,因此从市场规模也随之上升。根据头豹研究院整理,ADC药物的市场规模预计在2024年有望达到74 亿元,2030年预计市场规模达到292亿元人民币,2024-2030年复合增长率为25.71%。

国家卫生健康委发布最新公告显示,2020年各类传播途径的甲乙类传染病发病率均呈现明显下降,其中肠道传染病发病率较2019年下降29.4%、呼吸道传染病发病率较2019年下降12.9%。因此,全球,包括中国在内的抗菌药物的使用额呈下降趋势。
随着新药的不断研发和政策的完善,渐冻症治疗市场有望迎来更加广阔的发展前景。