
News information
分类:行业资讯 发布时间:2023-10-24 访问量:1337
前 言
据国际罕见病日官网数据显示,全球罕见病患者超过3亿人,约占全球总人口的3.5%至5.9%,严格意义上来讲“罕见病或许并不罕见”,而如此巨大的临床需求之下,全球研发管线中也有超过1/3比例属于了“罕见病新药”研究,令人震惊。
目录的发布从另一方面来讲也为我国加强罕见病管理、提高罕见病诊疗水平、维护罕见病患者健康权益提供了充分的法律依据,对于未来罕见病诊疗保障事业的推动、促进药物可及、健全患者保障体系具有重要指导意义。
细节上,此次发布的《第二批罕见病目录》中共涉及了86个罕见病种,叠加第一批目录下的121种罕见病,两批目录目前已收录了207种罕见病。
同时,在第二批罕见病目录中,也有不少重点内容值得提及,即有超过29种罕见病的40+创新药已经在国内获批上市,10+种罕见病新药即将上市,更有超过18种罕见病领域国内尚无一家药企布局。
29种罕见病国内新药已上市
首先,针对《第二批罕见病目录》中公布的疾病种类,统计相关疾病的海内外新药获批情况,发现至少有29种罕见病国内目前已有新药上市(不完全统计),其中不仅有肢端肥大症、新生儿肺动脉高压、幼年特发性关节炎等遗传学疾病,更有皮肤T细胞淋巴瘤、骨巨细胞瘤、神经母细胞瘤等高发“罕见肿瘤”疾病。
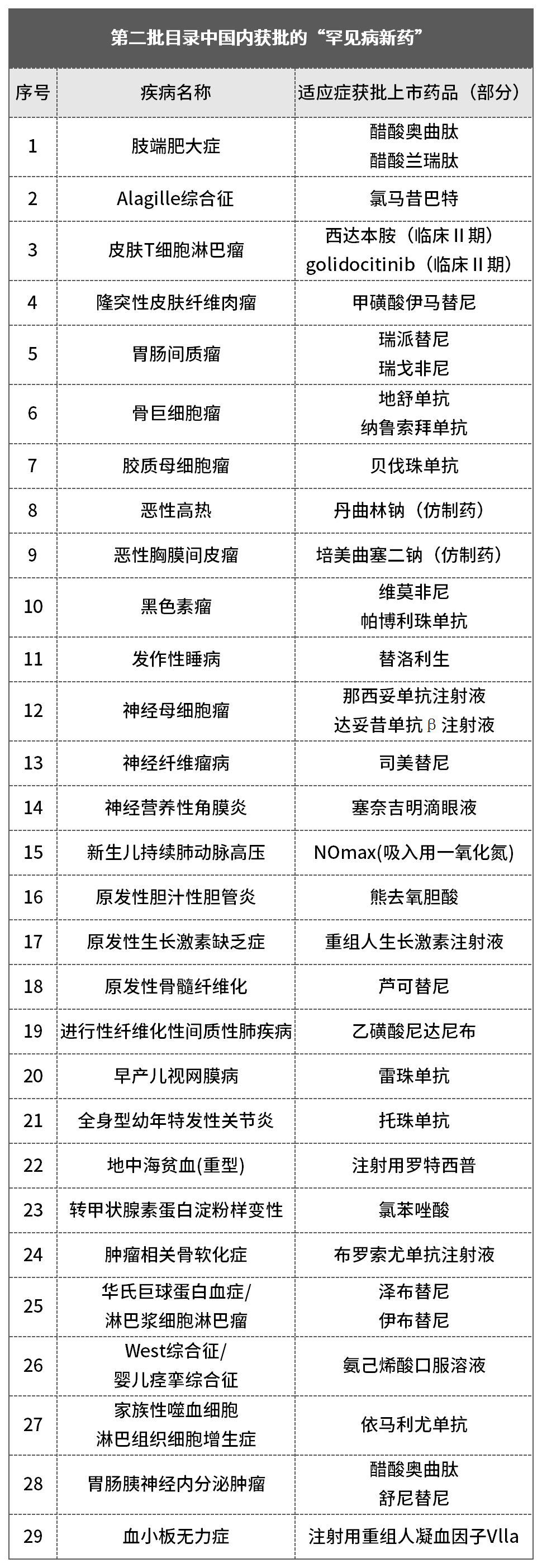
在全球3亿罕见病患者的巨大市场驱动下,海内外虽不断有罕见病新药成功上市,但整体上仍超过90%的罕见病尚无治疗方法,这也导致“罕见病新药研究”成为了现阶段医药探索和疗法研发的重点领域之一。
而事实上,有关资料也显示近年来FDA药物评估与研究中心(CDER)批准的新药中,有超过50%的比例均为罕见病,罕见病适应症研究占据了全球新药临床管线的3成,足见其重大趋势。
18种罕见病“境外有药,境内无药”
除了上述罕见病目录中的“有药可用”的情况,其实罕见病目录中更多仍是“境外有药,境内无药”的情况,据药智数据显示,不完全统计之下,目录中至少有18种罕见病在国内尚无相关适应症的研究布局,其中不乏梅克尔细胞癌、早衰病、巨细胞动脉炎、神经元蜡样质沉积症等临床新药需求迫切的领域。
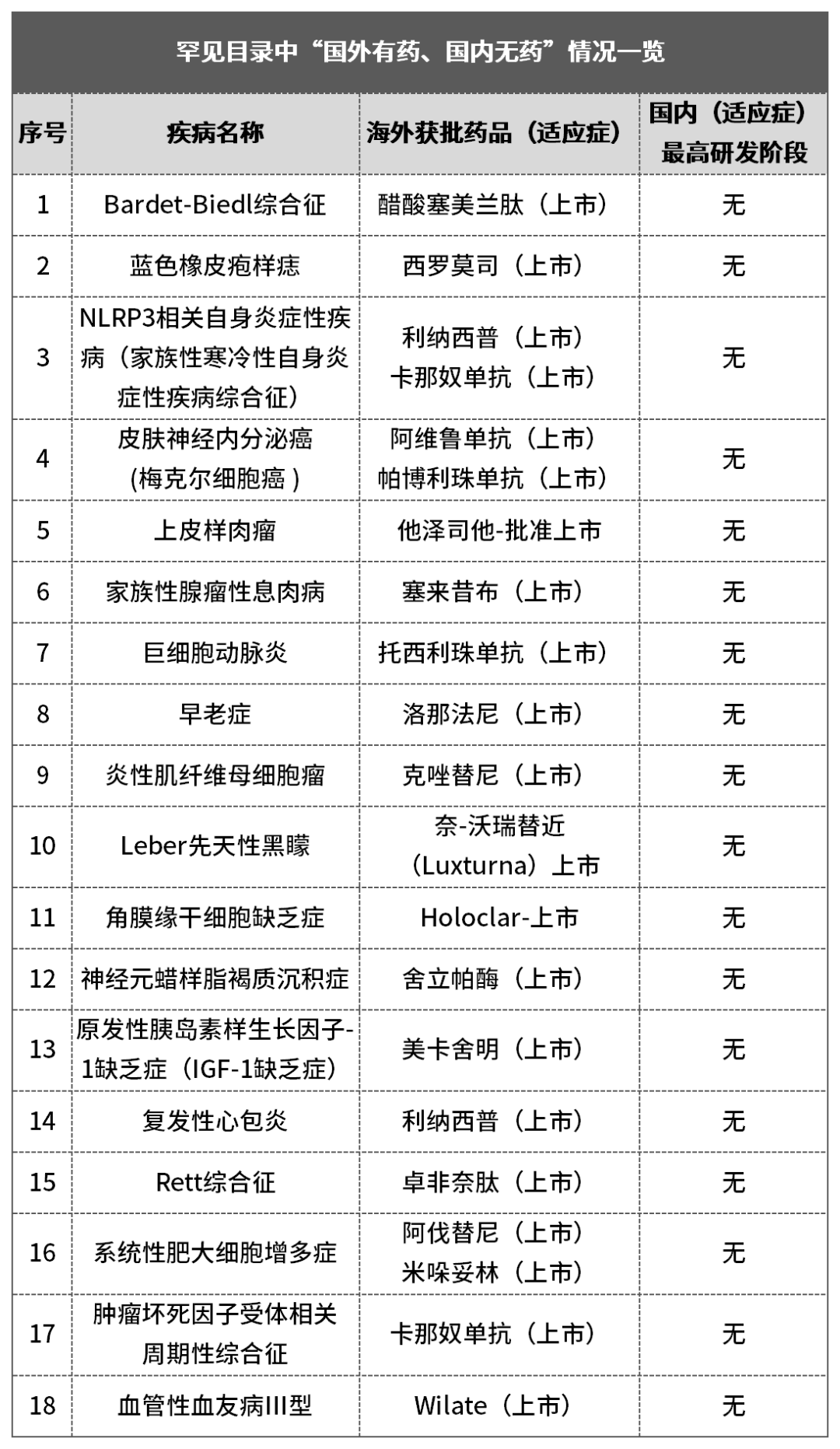
对于这部分罕见病而言,海外上市情况多为局部地区(不仅限于美国FDA,也包括欧盟、日本、韩国等),在此基础上,虽然国内领域的罕见病适应症并未获批,但仍可以依靠相关获批药品的超适应症用药来曲线救国。
但整体来讲,这部分的临床需求相对迫切,对于国内药企而言,借此次纳入第二批罕见病目录,或许也可以选择在避开愈发同质化愈发严重的常规创新药市场,转而积极拓展罕见病适应症的新药开发。
10+种罕见病“新药”国内即将上市
最后,在罕见病目录中还有更值得一提的,即有超过10款罕见病新药或将在未来短时间内在国内获批上市。

总 结

国家医保部门从多个方面考虑到参保人员的利益,进而对相关政策进行调整和完善,提升居民的生活幸福感。

2020年-2025年,因新品上市以及患癌人数不断增加,因此从市场规模也随之上升。根据头豹研究院整理,ADC药物的市场规模预计在2024年有望达到74 亿元,2030年预计市场规模达到292亿元人民币,2024-2030年复合增长率为25.71%。

国家卫生健康委发布最新公告显示,2020年各类传播途径的甲乙类传染病发病率均呈现明显下降,其中肠道传染病发病率较2019年下降29.4%、呼吸道传染病发病率较2019年下降12.9%。因此,全球,包括中国在内的抗菌药物的使用额呈下降趋势。
随着新药的不断研发和政策的完善,渐冻症治疗市场有望迎来更加广阔的发展前景。